
タンパク質間ドッキングによる複合体モデリング
はじめに:タンパク質間相互作用(PPI)とは
シグナル伝達、細胞制御、分子認識といった生命活動の根幹を支えるプロセスにおいて、タンパク質複合体は重要な役割を担っています。 このような複合体の形成と安定化には タンパク質間相互作用(Protein-Protein Interaction; PPI) が関与しています。 これらの相互作用は、タンパク質ドメイン間の特異的な物理的接触によって駆動され、複合体ごとに多様な機能が発現します。
PPIの分子メカニズムを理解するためには、「分子同士がどのように結合し、結合親和性がどのように決定されるのか」を解明する必要があります[1,2]。 しかし、このような複合体の構造を実験的な手法で得るには、多大な手間と費用がかかるのが実情です。 コンピュータを用いた効率的なドッキングシミュレーションは、PPIの解析や予測に有効なアプローチとして注目されています[3,4]。

シミュレーション手法:タンパク質間ドッキング(PPD)
一般的な分子ドッキングの概要
タンパク質複合体などの分子複合体は、相互作用する2つ以上の分子によって形成されます。 これらの構造をモデル化するために、分子ドッキング と呼ばれるシミュレーション手法が用いられます。 非共有結合性の分子間相互作用を原子レベルで計算する事により、複合体の形成・安定化のプロセスがシミュレートされます[6]。 分子ドッキング法は、「複合体自体の構造は不明であるものの、個々の構成要素(分子サブユニット)の立体構造が既知あるいは予測可能である」という場合に有効な手法です。
剛体アプローチを用いたタンパク質間ドッキング
タンパク質間ドッキング(Protein-Protein Docking; PPD) は、相互作用面が大きく平坦かつ疎水性が高い傾向にあるため、一般的なドッキングシミュレーションよりも複雑になります。 この複雑さは、タンパク質特有の柔軟性や、変化しうる構造(コンフォメーション空間)の広大さに起因します。 また、結合部位が広範囲にわたるため、配向探索アルゴリズムも「タンパク質-リガンドドッキング」で用いられるものとは異なる手法が選ばれます。
一般的には、まず分子を剛体とみなして膨大な数の配向パターンを探索し、その後にエネルギー最小化や柔軟性を取り入れた精緻化(最適化)を行います。 剛体アプローチは、構成タンパク質(あるいはその近縁相同体)とそれらの複合体について、高解像度の結晶構造データが利用できる場合に適用されます[7,8]。
- タンパク質間ドッキング(PPD)の主な応用例[9-12]:
- タンパク質間相互作用(PPI)経路の標的化と阻害
- 抗体と抗原の相互作用解析
- がん関連経路の調節
- 宿主と病原体の相互作用研究
- ネットワーク薬理学研究
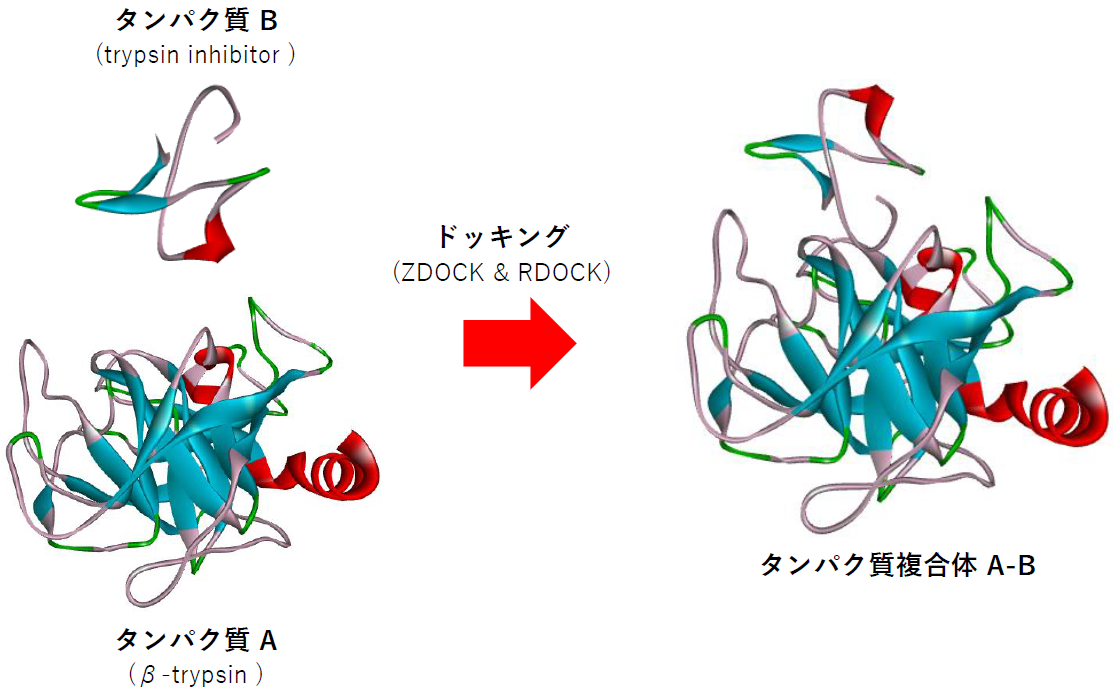
シミュレーション事例: ZDOCK を用いたタンパク質間ドッキング
ZDOCK は、タンパク質-タンパク質の2分子系における6つの空間自由度(回転3自由度および並進3自由度)を効率的に探索する、剛体ドッキングアルゴリズムです。 通常は、柔軟性も考慮する RDOCK と組み合わせて、次の2ステップでモデリングと解析が進められます[13,14]。
- ドッキングポーズの高速探索と評価( ZDOCK )
- ドッキングポーズの精緻化と再評価( RDOCK )
BIOVIA Discovery Studio では、これら2種のアルゴリズムによるドッキング処理を、UI画面上のツールパネルから簡単に実行できます。 以下の解析例では、それらの機能を使用して、 ウシ膵臓由来のβ-トリプシン(タンパク質受容体)とカボチャ種子由来の阻害剤CMTI-I(タンパク質リガンド)の複合体モデルを作成しました[15,16]。 なお、この複合体のX線結晶構造は既に知られています[17]。
ドッキングポーズの高速探索と評価( ZDOCK )
最初の探索ステップでは、受容体とリガンドの各タンパク質を剛体として扱います。 ZDOCK のスコアリングでは、ペアワイズ形状相補性(Pairwise Shape Complementarity; PSC)が評価されます[13]。 PSCは、ある原子間距離における近接接触をペアワイズ法で計算するアプローチであり、表面曲率を考慮した高精度な評価と高速探索を両立させます。
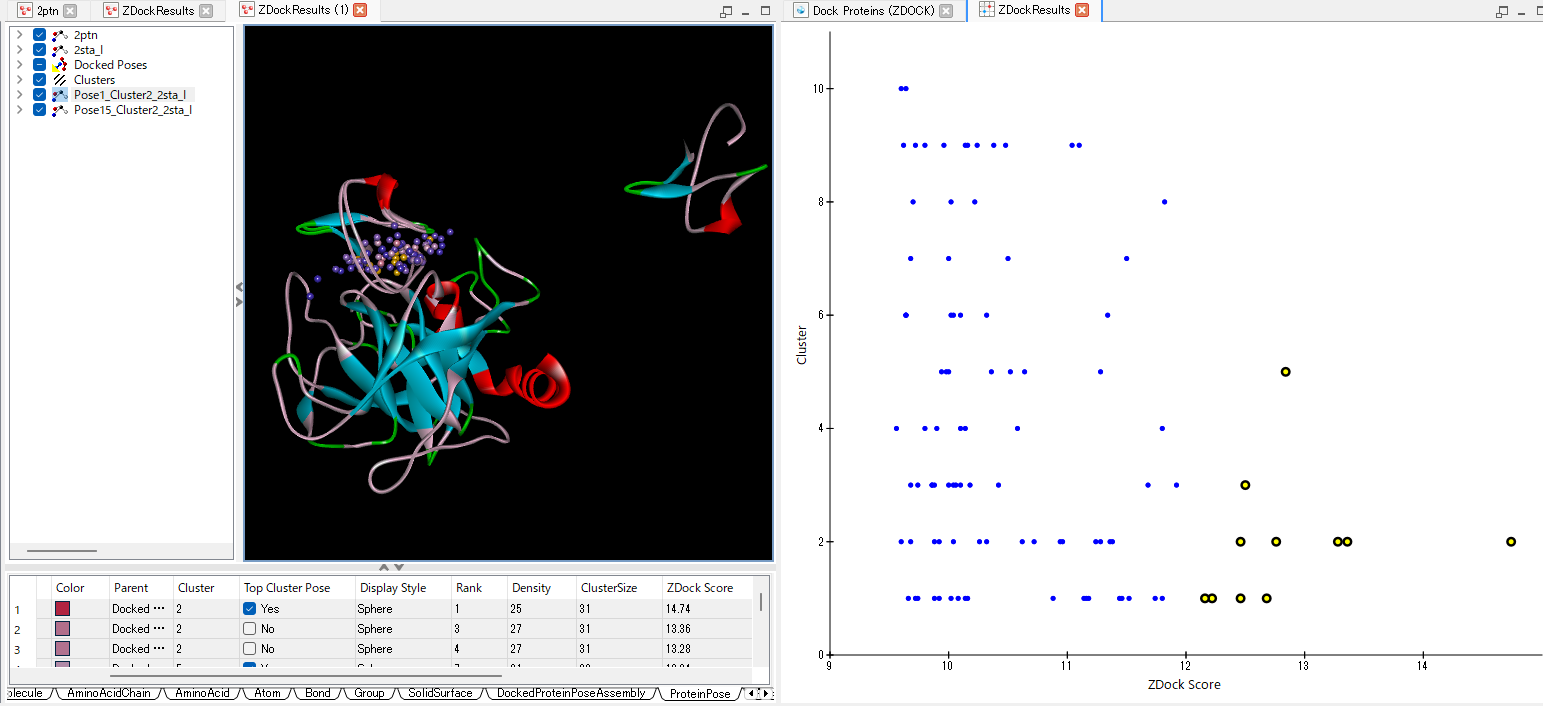
ZDOCK では、類似構造のポーズは自動的にクラスタリングされてから出力されます。 上図の3Dビューとテーブル(左)には、スコアが上位のクラスター(10グループ)に含まれるポーズ(100種)が示されています。 2Dプロット分析(右)からは、上位ポーズがどのグループに集中しているか、がわかります。
この事例ではスコア12.0を超えるポーズが11種確認されました(黄色の点)。 これらの複合体構造に対して、次の RDOCK で精緻化を行います。
ドッキングポーズの精緻化と再評価( RDOCK )
RDOCK は、ZDOCK で得られた複合体構造をさらに精緻化するためのアルゴリズムです。 ZDOCK で絞り込まれた数十~数千のニアネイティブ構造(真に近い構造)を対象とし、安定構造の再計算と再評価を行います。
RDOCK による構造最適化とスコアリングでは、CHARMm 力場ベースのエネルギー関数が採用されています[18]。 ここではコンフォメーション変化を許容して、立体障害を除去し、極性相互作用とイオン性残基の電荷相互作用を最小化します。 そして最適化された全ての構造に対して、静電相互作用エネルギーと脱溶媒和エネルギーを計算し、それらの合計値に基づいて構造を再評価します。
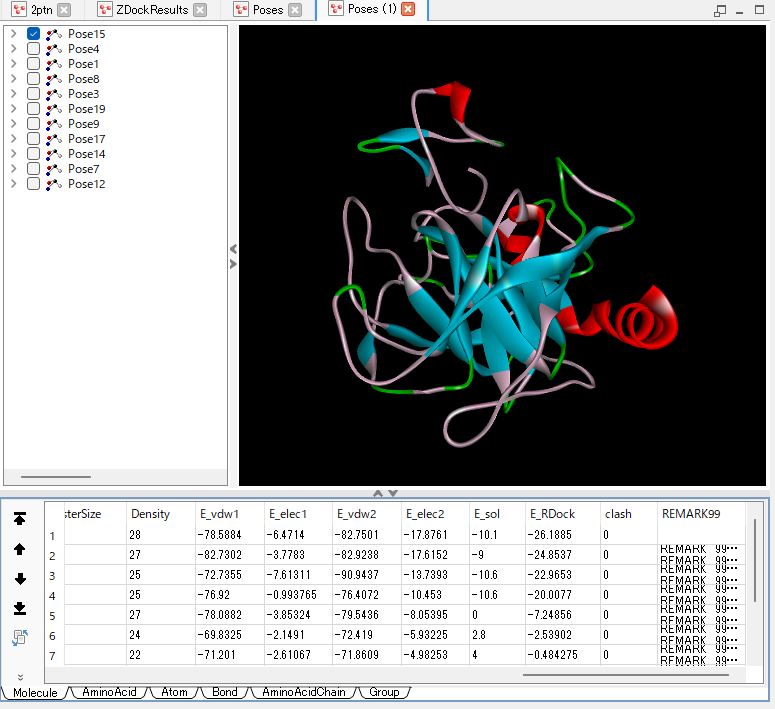
この図には、精緻化された各ポーズの結果が表示されています。 データを解釈するために、RDOCK が算出した各種エネルギー値が下側のテーブルに一覧表示されます。 このテーブルには ZDOCK 時のPSCスコアやクラスタリング情報も統合されており、多角的な結果の解釈に役立ちます。 各ポーズに対する複合体構造は、上側の3Dビューで視覚的に確認できます。
まとめ
本記事では、BIOVIA Discovery Studio のドッキング機能である ZDOCK (および RDOCK )を使用して、 タンパク質間複合体の安定構造を予測する手法を紹介しました。 本製品には、更なる解析・分析・評価のためのツール群や、他にも様々なドッキング機能が備わっています。 もしご質問・ご要望がございましたら、弊社ウェーブフロントまで お問い合わせ ください。
参考文献
A. H. Santoyo, et al. (2013), "Protein-Protein and Protein-Ligand Docking", Protein Engineering: Technology and Application, Intechopen, DOI:10.5772/56376
Topics of "Protein-Protein Interaction", ScienceDirect, URL:sciencedirect.com/topics/biochemistry-genetics-and-molecular-biology/protein-protein-interaction
H. Nada, et al. (2024), Sig. Transduct Target Ther., 9(1): 341, DOI:10.1038/s41392-024-02036-3
T. Schwede (2013), Structure, 21(9): 1531-1540, DOI:10.1016/j.str.2013.08.007
H. Elhabashy, et al. (2022), Structure, 30(4): 462-475, DOI:10.1016/j.str.2022.02.004
X. Y. Meng, et al. (2011), Curr. Comput. Aided Drug Des., 7(2): 146-157, DOI:10.2174/157340911795677602
Topics of "Docking Protein", ScienceDirect, URL:sciencedirect.com/topics/pharmacology-toxicology-and-pharmaceutical-science/docking-protein
K. Roy, S. Kar, R. N. Das (2015), "Chapter 10 - Other Related Techniques", Understanding the Basics of QSAR for Applications in Pharmaceutical Sciences and Risk Assessment, Academic Press, 357-425, DOI:10.1016/B978-0-12-801505-6.00010-7
R. Sable and S. Jois (2015), Molecules, 20(6): 11569-11603, DOI:10.3390/molecules200611569
Q. U. A. Farooq, et al. (2021), World J. Virol., 10(6): 288-300, DOI:10.5501/wjv.v10.i6.288
R. Yuan, et al. (2025), Mol. Ther., 33(5): 2252-2268, DOI:10.1016/j.ymthe.2025.04.003
S. H. Hong, et al. (2025), Chem. Rev., 125(14): 6819-6869, DOI:10.1021/acs.chemrev.5c00046
R. Chen, L. Li, and Z. Weng (2003), Proteins, 52(1): 80-87, DOI:10.1002/prot.10389
Topics of "Fast Fourier Transform Algorithm", ScienceDirect, URL:sciencedirect.com/topics/engineering/fast-fourier-transform-algorithm
J. Walter, et al. (1982), Acta. Cryst., B38(5): 1462-1472, DOI:10.1107/S0567740882006153
R. Helland, et al. (1999), Acta. Cryst., D55: 139-148, DOI:10.1107/S090744499801052X
W. Bode, et al. (1989), FEBS Lett., 242(2): 285-292, DOI:10.1016/0014-5793(89)80486-7
L. Li, R. Chen, and Z. Weng (2003), Proteins, 53(3): 693-707, DOI:10.1002/prot.10460
記事制作者
- 執筆:
- ララサティ・マルタ (株式会社ウェーブフロント 連成問題研究部)
- 佐橋 一裕 (株式会社ウェーブフロント 連成問題研究部)
- 編集:
- 佐橋 一裕 (株式会社ウェーブフロント 連成問題研究部)
